Prvo galvansko celico na svetu je razvil Luigi Galvani. Preberite o njeni zgodovini. v tem člankuV bistvu gre za začasni vir električnega toka, ki ga ustvari kemična reakcija. Tok elektronov nastane z interakcijo med dvema različnima kovinama. Posledično se kemična energija pretvori v električno energijo, ki jo lahko nato uporabimo v vsakdanjem življenju.
Koncentracijska galvanska celica je vir toka, ki ga sestavljata dve enaki kovinski elektrodi, nameščeni v mešanici soli te kovine v različnih koncentracijah.
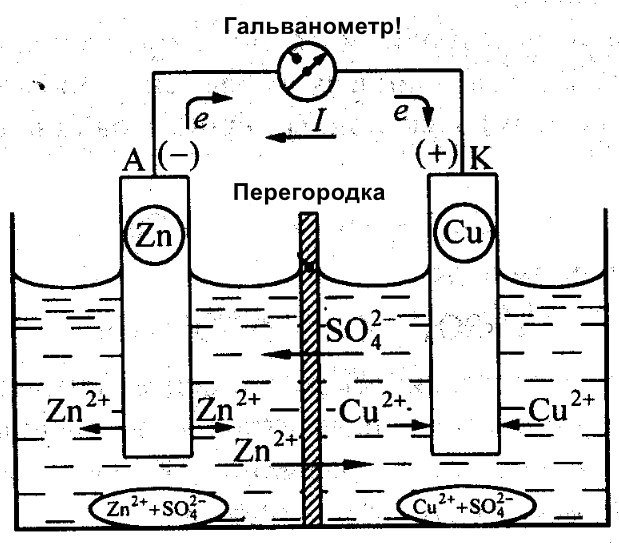
Poleg Galvanija je na ustvarjanju učinkovite baterije delal tudi Daniel Jacobi. Svoj vir energije je nekoliko spremenil. Sestavljen je iz bakrene plošče, nameščene v CuSO4, in cinkove plošče, potopljene v ZnSO4. Da bi preprečili njuno neposredno interakcijo, je med njima nameščena porozna stena. Spodaj je diagram galvanske celice Daniela Jacobija.
Cink in baker imata različno reaktivnost, zato se bosta razlikovala tudi pri naboju. Posledično tudi nivoji elektrod niso enakomerni. To jim omogoča, da se premikajo in ustvarjajo električni ali galvanski tok. Ta tok začne teči, ko oseba ali izumitelj naprave za shranjevanje toka priključi obremenitev. Ta obremenitev je lahko žarnica, radio, računalniška miška ali druge električne naprave.
Shematski diagram galvanske celice
Vezni diagram se nanaša na njegovo sestavo in strukturo. Z uporabo pomožnih naprav ga je mogoče sestaviti iz več kemičnih elementov. Spodaj bo na kratko opisana struktura galvanske celice. Več o tem si preberite v tem članku.!
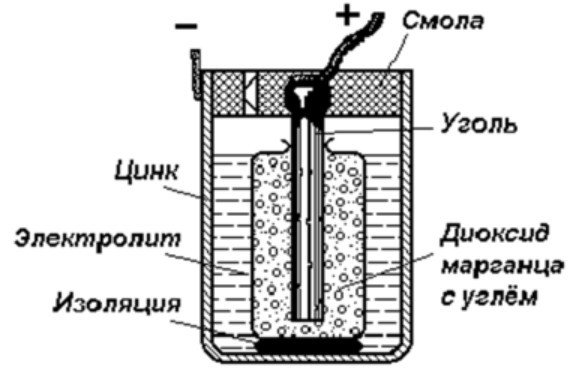
Struktura galvanske celice
Najenostavnejša naprava za shranjevanje energije je sestavljena iz:
- Palica premoga.
- Dve različni kovini.
- Elektrolit.
- Smola ali plastika.
- Izolator.
Kot je razvidno iz tega diagrama, je galvanska celica sestavljena iz negativne in pozitivne elektrode. Lahko sta izdelani iz bakra, cinka ali drugih kovin. Imenujejo se bakreno-cinkove celice. Včasih se imenujejo suhe baterije.
Oznaka galvanske celice na diagramu Izdelana je v obliki dveh navpičnih črt, ki sta blizu druga drugi na majhni razdalji. Ena od njiju bo manjša. Na robovih vsake take črte so znaki, ki označujejo polarnostDolga črta je označena s pozitivno, kratka pa z negativno. Zraven je lahko prikazana napetost. To pomeni, da vezje, ki uporablja baterijo, deluje samo pri tej napetosti.
Načelo delovanja galvanske celice
Galvanska celica deluje s premikanjem elektronov z enega kovinskega kontakta na drugega. Pri tem pride do kemične transformacije. Preberite več o termodinamiki galvanske celice in nastanku galvanske elektrike. Tukaj.
Odgovori na pogosto zastavljena vprašanja
| Galvansko | Razlaga |
| Baterija | Vir energije, ki deluje s procesi, ki se odvijajo v omejenem, miniaturnem prostoru. Natančneje, energija se proizvaja s kemično reakcijo. |
| Voltaična celica ali Voltaični kup | To je energijski element, ki ga je prvi ustvaril znanstvenik po imenu Volt. |
| Postopek | Interakcija med kemičnimi elementi, ki povzroči nastanek električnega toka. |
| Izpust | To je zaključek kemične reakcije. To pomeni, da med snovmi ne bo interakcije. Galvanski razelektritev je prisotna v Warframeu. V bistvu gre za modifikacijo, ki je primanjkuje. Uporablja se za orožje za bližnji boj. PolarnostV2. |
| Galvanski kontakt | To je stik med elektrodami in raztopino. |
| Učinek | Pojav razlike med dvema stikoma, izdelanima iz dveh vrst kovin. Velikost je odvisna od temperature in kemijske sestave prevodnikov. V bistvu je to Voltov prvi zakon. |
| Povezava/člen/veriga | Povezava dveh ali več delov električnega tokokroga z virom toka. |
| Galvanski naboj | Polnjenje baterije z energijo. |
Galvanizacija je kemični postopek z uporabo električnega toka. Reakcija zmanjša količino raztopljenih kovinskih kationov do te mere, da sčasoma tvorijo enakomerno prevleko na kovinski elektrodi. Posledično izdelek postane bolj trpežen, majhne vdolbine izginejo, njegov videz pa postane privlačnejši.
Vrste galvanskih celic
Obstaja več specifičnih vrst baterij.
Tabela galvanskih členov
| Vrsta | Napetost | Glavne prednosti |
| Litij | 3 V | Velik zmogljivost, visok tok. |
| Solne baterije ali ogljik-cinkov | 1,5 palca | Najcenejši. |
| Nikljev oksihidroksil NiOOH | 1,6 volta | Visok tok. Visoka zmogljivost. |
| Alkalno ali alkalno | 1,6 V | Visok tok. Dobra glasnost. |
Ta tema je podrobneje obravnavana v članku. vrste baterij!
Namen galvanske celice
Namenjen je zagonu električne opreme. Ta lahko vključuje:
- Pazi.
- Daljinski upravljalniki.
- Svetilke.
- Medicinska oprema.
- Prenosniki.
- Igrače.
- Obeski za ključe.
- Telefoni.
- Laserski kazalci.
- Kalkulatorji.
In podobne stvari okoli nas.
Galvanska celica doma
Preprost vir napajanja lahko izdelate sami. Za to boste potrebovali naslednje materiale:
- Plastična skodelica.
- Elektrolit. To je lahko fiziološka raztopina, soda ali citronska kislina, razredčena v vodi.
- Plošče iz dveh različnih kovin. Na primer aluminija in bakra.
- Žice
Proizvodni proces
Vzemite plastično skodelico in vanjo nalijte elektrolit. Ne napolnite je do roba; najbolje je, da jo pustite 1-2 centimetra kratko. Žice pritrdite na kovinske plošče. Nato bakrene in aluminijaste plošče položite na robove posode. Morajo biti vzporedne druga z drugo. Ko je vse pripravljeno, lahko napetost izmerite z voltmetrom.
Priključite napravo in se dotaknite sond na kontakte našega vira napajanja. Držite jih na mestu, dokler se na zaslonu ne prikaže napetost. Običajno je to 0,5-0,7 volta. Te vrednosti so odvisne od elektrolita oziroma natančneje od snovi, ki se uporablja kot elektrolit.
Takole je narejena domača galvanska celica.